г. Москва и Московская область, Россия
Россия
ВАК 3.1 Клиническая медицина
ВАК 3.1.10 Нейрохирургия
Послеродовая анальная инконтиненция часто связана с повреждением сфинктерного аппарата и нервных структур, что определяет вариабельность клинического течения и ответ на терапию. Сакральная нейростимуляция является эффективным методом лечения, однако влияние анатомической целостности сфинктера на результат остаётся недостаточно изученным. В ретроспективном исследовании оценивали эффективность нейростимуляции у женщин с послеродовой инконтиненцией при сохранённом сфинктере и при его разрыве, анализируя динамику симптомов, качества жизни и сексуальной функции. Наиболее выраженный терапевтический эффект наблюдался у пациенток без структурного дефекта, тогда как при наличии разрыва улучшения были ограниченными. Полученные данные указывают, что сакральная нейростимуляция наиболее результативна при сохранённой анатомии сфинктера, что позволяет рассматривать возможность прямой имплантации стимуляционной системы без предварительного тестового этапа у соответствующей категории пациенток.
Анальная инконтиненция, стимуляция крестцовых корешков (SNRS), травма анального сфинктера
Резюме
Введение. Недержание газов и/или кала часто ассоциировано с повреждение анального сфинктера и половых нервов после физиологических родов. Частота послеродовой анальной инконтинеции (АИ) варьируется от 3,8% до 19,4%. Нейростимуляция крестцовых корешков (сакральная нейростимуляция, SNRS) является одним из методов лечения АИ, при неэффективности иных методов лечения. Несмотря на распространенность и доказанную эффективность данного метода в лечении анальной инконтиненции различного генеза вопрос о предикторах эффективности нейростимуляции остается открытым. Данное исследование направлено на оценку эффективности SNRS у женщин с послеродовой дисфункцией анального сфинктера в зависимости от наличия разрыва анального сфинктера в анамнезе.
Материалы и методы. Было проведено ретроспективное наблюдательное исследование, направленное на оценку эффективности сакральной электростимуляции у женщин с послеродовой анальной инконтиненцией (АИ). Пациенток распределяли на две клинические подгруппы: группа 1 — пациентки с клинически значимой АИ без разрыва анального сфинктера; группа 2 — пацинетки с клинически значимой АИ с разрывом анального сфинктера
Основным параметром, по которому определяли успешность лечения, служило изменение степени недержания по шкале Wexner. Терапевтический ответ считался достигнутым при снижении выраженности симптомов не менее чем на 50% относительно исходного уровня. Состояние пациенток оценивали в динамике — через 3, 6 и 12 месяцев после имплантации.
Дополнительными, вторичными, критериями выступали показатели качества жизни и сексуального благополучия, определённые с использованием валидизированных опросников FIQL и PISQ.
Результаты. У пациенток без разрыва сфинктерного комплекса наблюдались выраженные улучшения по всем ключевым шкалам. За год после начала стимуляции среднее значение Wexner уменьшилось с 14,5±2,0 до 4,25±3,3 (p=0,0001). Показатели PISQ снизились с 23,375±3,8 до 9,375±3,1 (p=0,0003), что отражает позитивную динамику сексуальной функции. Средний балл FIQL увеличился с 1,76±0,18 до 3,575±0,4 (p=0,0062), что соответствует существенному росту качества жизни у данной группы.Таким образом, наличие анатомического дефекта сфинктера существенно ограничивает эффективность метода, хотя определённые клинические улучшения у этих пациенток также фиксируются.
Заключение. Сакральная нейростимуляция демонстрирует выраженное улучшение контроля дефекации у женщин с послеродовыми повреждениями анального сфинктера. Наибольший терапевтический эффект наблюдается у пациенток, у которых не выявлено структурного разрыва сфинктерного аппарата: степень инконтиненции по шкале Wexner снижается в среднем на 70% по сравнению с 13% в группе с разрывом; показатели PISQ улучшаются на 60% против 21%; параметры FIQL — на 51% против 12,5%.
С учётом столь высокой эффективности процедуры при сохранённой анатомической целостности сфинктера, а также ограниченной диагностической ценности длительного тестового периода у пациенток, страдающих преимущественно недержанием жидкого стула и газов, представляется оправданным рассматривать возможность прямой имплантации стимуляционной системы без предварительного тестового этапа для перечисленных категорий больных.
Введение
Физиологическое родоразрешение может приводить к повреждению мышц анального сфинктера и нервных структур тазового дна, что проявляется различными нарушениями функции тазовых органов (НФТО), включая недержание газов и/или кала — анальную инконтиненцию (АИ), а также формирование хронического болевого синдрома в области промежности [1]. Согласно литературным данным, разрывы сфинктерного комплекса осложняют около 3,8% всех вагинальных родов, но при наличии отягощающих факторов — таких как наложение акушерских щипцов, применение вакуум-экстрактора, эпизиотомия или разрывы промежности III–IV степени — частота возрастает почти до 19,4% [2]
При этом даже при отсутствии явных разрывов мягких тканей длительный или стремительный родовой период, а также натяжение нервных стволов могут вызывать скрытые повреждения сфинктера или нейропатию, которые клинически проявляются спустя время. Ряд исследований свидетельствует, что у примерно одной трети первородящих выявляются ранее не диагностированные нарушения анатомии или функции сфинктерного аппарата [3]
Такие травмы приводят к комплексу симптомов — от ложных позывов (тенезмов) и эпизодов недержания до хронической тазовой боли, зачастую сопровождающейся диспареунией. Эти проявления существенно ухудшают качество жизни, ограничивают бытовую и социальную активность женщины и затрудняют уход за новорождённым ребёнком [1]
Консервативные и реабилитационные подходы — такие как изменение образа жизни, корректировка рациона, тренировка мышц тазового дна, применение методов биологической обратной связи — традиционно являются первым этапом лечения послеродовой дисфункции сфинктерного аппарата. Однако при выраженной или стойкой анальной инконтиненции их эффективности бывает недостаточно, и возникает необходимость в хирургической коррекции. Наиболее распространённым оперативным вмешательством остаётся сфинктеропластика, но её долговременные результаты нередко снижаются: у значительного числа пациенток спустя несколько лет наблюдается возврат симптомов, что стимулирует поиск альтернативных терапевтических решений [3].
За последние десятилетия сакральная нейромодуляция заняла значимое место в лечении рефрактерного анального недержания [4]. Метод электростимуляции крестцовых корешков (SNRS, sacral nerve root stimulation) предусматривает имплантацию электрода в области крестца, чаще всего на уровне корешка S3, с подачей постоянных электрических импульсов, влияющих на рефлекторные дуги, участвующие в контроле аноректальной функции [5]. Хотя механизмы действия SNRS полностью не раскрыты, предполагается, что стимуляция улучшает активность внешнего анального сфинктера, усиливает функциональные возможности мышц тазового дна и повышает пороги чувствительности прямой кишки [6].
Метод относится к малоинвазивным, обратимым и хорошо переносимым вмешательствам и рассматривается как один из ведущих способов терапии АИ при отсутствии эффекта от консервативных методов [7]. Согласно данным Thin NN и соавт., даже при наличии анатомических повреждений сфинктерного комплекса у женщин возможно достижение значимого улучшения контроля дефекации при использовании SNRS [4]. Кроме того, нейромодуляция способна уменьшать выраженность тазовой боли, что связывают с модификацией афферентных болевых путей [4].
Крупнейшее исследование, проведённое при участии FDA, показало, что пробная стимуляция была успешной у 90% из 133 пациентов; постоянные системы были установлены 120 из них. Терапевтический эффект отмечен у 83% больных, причём у 41% инконтиненция исчезла полностью. Спустя два года после имплантации у 85% пациентов улучшение сохранялось [7].
Данные литературы, а также наши собственные наблюдения подтверждают, что SNRS обеспечивает выраженные клинические улучшения у женщин с послеродовым недержанием кала и газов [8]. Метод эффективно снижает частоту эпизодов инконтиненции и повышает способность к произвольному контролю дефекации [4].
Несмотря на широкую распространённость сакральной нейростимуляции, остаётся нерешённым вопрос о факторах, определяющих успешность лечения. В частности, недостаточно изучено, как наличие разрыва анального сфинктера влияет на результативность метода. В связи с этим нами проведено исследование, целью которого стало определение эффективности SNRS у женщин с послеродовой дисфункцией анального сфинктера с учётом наличия либо отсутствия сфинктерного дефекта в анамнезе.
Материалы и методы
Проведено ретроспективное исследование эффективности SNRS у женщин с послеродовой дисфункцией анального сфинктера за период с 2021 по 2023гг.
Критерии включения:
- Возраст пациентки ≥ 18 лет;
- Больные с нарушением функции тазовых органов в виде недержания газов и/или кала;
- Неэффективность адекватной консервативной терапии сроком не менее 3 месяцев.
Критерии невлючения:
- Наличие эндогенных психических заболеваний;
- Наличие абсолютных показаний для проведения сфинктеропластики или иной «анатомической» операции;
- Отказ от участия в исследовании на любом из этапов исследования.
Ключевыми точками для оценки состояния пациенток были следующие: до операции, в ранний послеоперационный (п/о) период (1-2 недели после операции), спустя 3, 6 и 12 месяцев после операции.
Состояние пациенток оценивалось по:
- Wexner Score – шкала оценки недержания кала в баллах от 0 до 20, где 0 – нет признаков недержания, а 20 – постоянное недержание как газов, так и жидкого и твердого стула с необходимостью использования прокладок или памперсов и с сильным влиянием на стиль жизни;
- PISQ-IR (Pelvic Organ Prolapse/Urinary Incontinence SexualQuestionnaire, IUGA-Revised) – опросник оценки сексуальной функции у пациентов с НФТО от 2 до 36 баллов, где 2 это нет проявлений сексуальной дисфункции, а 36 – очень выраженная сексуальная дисфункция;
- FIQL (Fecal Incontinence Quality of Life Scale) – шкала оценки качества жизни, связанное с недержанием кала, в котором содержатся 29 вопросов по оценке качества жизни, на каждый из которых можно дать ответ от 1 (полностью согласен) до 4 (полностью не согласен), результатом является среднее значение этих ответов. Чем выше количество баллов, тем выше качество жизни пациенток.
Анализ полученных данных проводился в программе «Statistica» с использованием непараметрических показателей. Проверку статистической значимости результатов проводили с использованием непараметрических процедур (критерий Крускала-Уоллиса, Вилкоксона, конкорданция Кендалла). Критическим уровнем статистической значимости был принят p <0,05.
В исследование вошли 13 пациенток, прооперированных в период с января 2021 по декабрь 2023гг. Средний возраст пациенток составил 32±9 полных лет. Время с момента появления симптомов до операции составило от 8 месяцев до 11 лет, в среднем 48 месяцев. Пациентки были разделены на 2 группы. Группа 1 – пациентки без разрыва анального сфинктера (8 пациенток), группа 2 – пациентки с разрывом сфинктера в анамнезе (5 пациенток), без абсолютных показаний к проведению сфинктеропластики (2 пациентки), а также с сохранением симптомов после проведения реконструктивной операции (2 пациентки), или отказавшиеся от данной операции (1 пациентка). Разрыв сфинктера определялся врачом-проктологом на основании физикального осмотра. Показания к нейростимуляции ставили также совместно с врачом проктологом на основании клинико-анамнестических данных, проведенного ранее консервативного, и в некоторых случаях хирургического лечения.
Все стадии исследования соответствовали законам Российской федерации, международным этическим нормам, одобрение локального этического комитета не требуется, все участники исследования дали информированное добровольное согласие на участие в исследовании и публикации.
При оценке однородности групп, статистически значимых различий между ними не выявлено. Среднее дооперационное значение степени инконтиненции по шкале Wexner в обеих группах составило 14,6±2,0 баллов (в группе 1 – 14,5±2,0 баллов; в группе 2 – 14,8±2,3 баллов), по опроснику PISQ среднее значение до лечения – 22,4±3,9 балла (группа 1 – 23,375±3,8 баллов; группа 2 – 20,8±4,0 баллов), и по шкале FIQL среднее – 1,78±0,2 баллов (группа 1 – 1,76±0,18; группа 2 – 1,82±0,23).
Пациенткам обеих групп проводилась имплантация электродов для стимуляции крестцовых корешков через отверстие S3 с одной или двух сторон (рис.1,2), или в крестцовый канал трансхиатально или ретроградно в зависимости от анатомии крестца и клинической картины. На выбор стороны стимуляции влияли такие факторы как степень развития крестцовых отверстий, желание и образ жизни пациента, визуализируемость отверстия S3 на рентгене. Значимой разницы в эффективности стимуляции в зависимости от стороны стимуляции нами выявлено не было. Необходимо отметить, что двустороннюю стимуляцию мы применяли только в 2 случаях, когда недержанию сопутствовала двустороння тазовая боль. В случае боли с одной стороны, электрод устанавливали с той же стороны, при отсутствии боли, у женщин только АИ сторона определялась вышеназванными факторами.
После проведения успешного тестового периода пациенткам имплантировался подкожный генератор импульсов в верхнеягодичную область. Для стимуляции использовали, как правило, специализированную под сакральную стимуляцию, систему InterStim II (фирмы Medtronic), но у пациенток с двусторонней тазовой болью в связи с необходимостью в имплантации двух электродов, применяли двухканальные системы (Montage фирмы Boston Scientific, а также Medtronic Intellis).
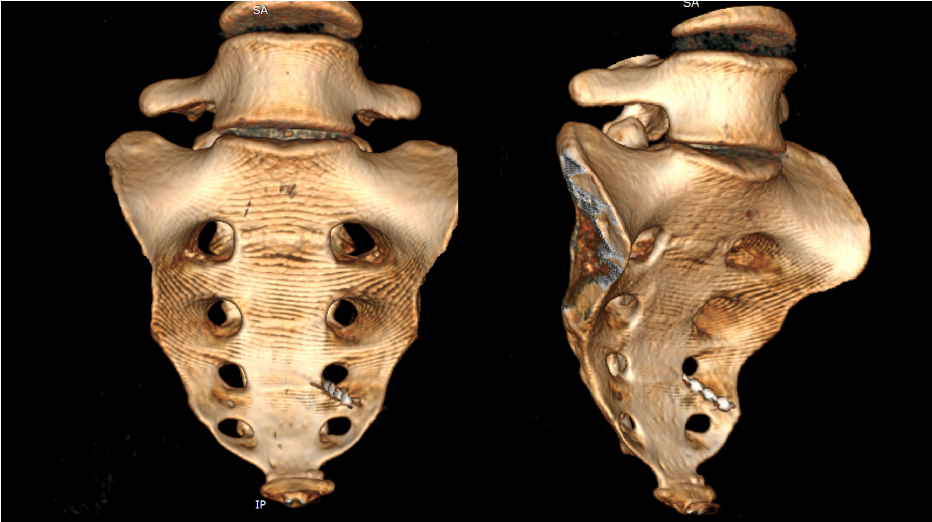 Рис. 1. 3D-реконструкция КТ крестца и копчика пациентки с имплантированным электродом для нейростимуляции S3 корешка слева по поводу послеродовой АИ.
Рис. 1. 3D-реконструкция КТ крестца и копчика пациентки с имплантированным электродом для нейростимуляции S3 корешка слева по поводу послеродовой АИ.
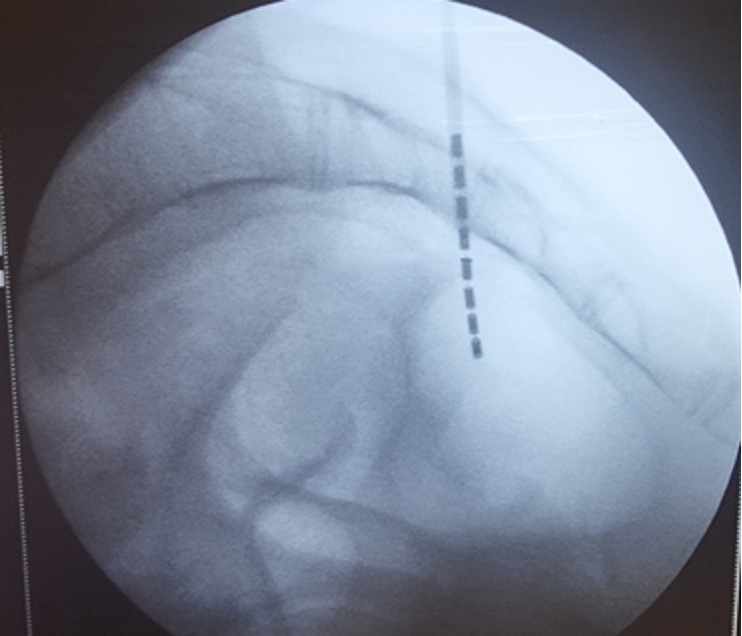
Рис 2. Рентгенограмма крестца в боковой проекции. Электрод располагается между 3 и 4 крестцовыми позвонками
Результаты
В ходе статистической обработки полученных данных установлено, что в первой группе пациенток наблюдалось как клинически, так и статистически значимое уменьшение выраженности симптомов анальной инконтиненции. Среднее значение по шкале Wexner снизилось с предоперационных 14,5±2,0 до 4,25±3,3 через 12 месяцев после внедрения системы нейростимуляции (p=0,0001), что указывает на выраженный терапевтический эффект.
Параллельно отмечено улучшение параметров сексуальной функции: показатели опросника PISQ уменьшились с 23,375±3,8 до 9,375±3,1 (p=0,0003). Существенные изменения затронули и качество жизни — средний балл FIQL увеличился с 1,76±0,18 до 3,575±0,4 спустя год после начала стимуляции (p=0,0062).
Пошаговая динамика всех измерений в ключевых временных точках, а также визуализация изменений симптомов представлена в таблице 31 и на рисунках №3 и №5.
|
Шкала |
До операции |
В ранний п/о период |
3 месяца после операции |
6 месяцев после операции |
12 месяцев после операции |
P-value |
|---|---|---|---|---|---|---|
|
Wexner |
14,5±2,0 |
6,25±2,9 |
4,625±3,3 |
4,25±3,3 |
4,25±3,3 |
0,0001 |
|
PISQ |
23,375±3,8 |
10,0±2,6 |
9,75±2,8 |
9,375±3,1 |
9,375±3,1 |
0,0003 |
|
FIQL |
1,76±0,18 |
3,50±0,59 |
3,51±0,53 |
3,55±0,46 |
3,575±0,4 |
0,0062 |
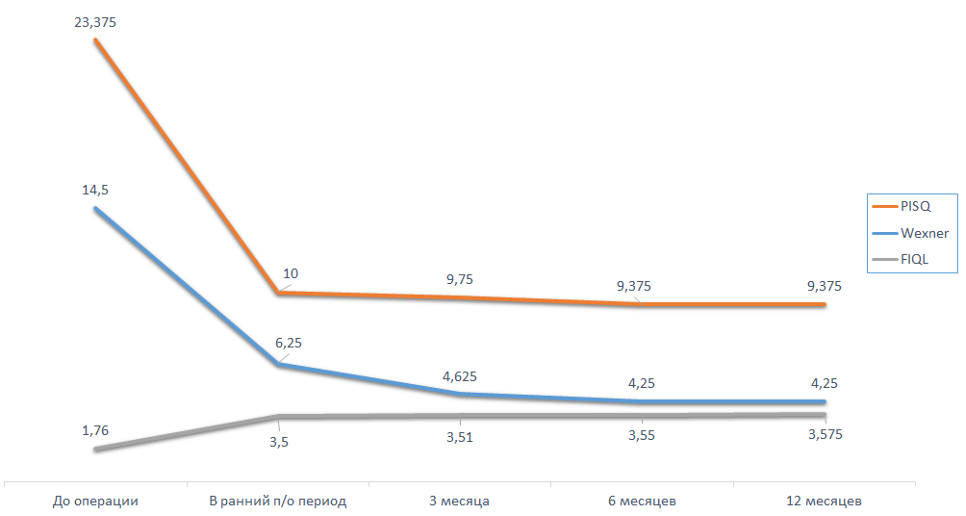 Рис.3 Динамика выраженности симптомом в группе 1
Рис.3 Динамика выраженности симптомом в группе 1
В группе с разрывом сфинктера нейростимуляция оказалась не столь эффективна. По шкале Wexner среднее значение баллов снизилось с 14,8±2,3 до 13,0±2,8 [p=0,1]. По опроснику PISQ – с 20,8±4,0 до 16,6±2,7[p=0,04]. По шкале FIQL – с 1,82±0,23 до 2,08±0,56 [p=0,1].. Баллы в каждой ключевой точке, а также динамика выраженности заболевания представлена в таблице №2, рисунках №4 и №5.
|
Шкала |
До операции |
В ранний п/о период |
3 месяца после операции |
6 месяцев после операции |
12 месяцев после операции |
P-value |
|---|---|---|---|---|---|---|
|
Wexner |
14,8±2,3 |
13,6±2,3 |
13,0±2,8 |
13,0±2,8 |
13,0±2,8 |
0,1 |
|
PISQ |
20,8±4,0 |
17,2±2,60 |
16,6±2,7 |
16,6±2,7 |
16,6±2,7 |
0,04 |
|
FIQL |
1,82±0,23 |
2,06±0,57 |
2,08±0,59 |
2,1±0,58 |
2,08±0,56 |
0,1 |
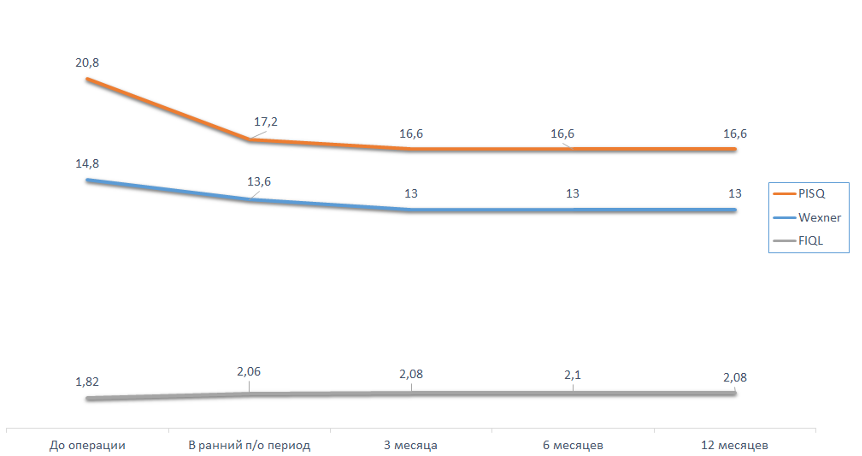
Рис.№4 Динамика выраженности симптомом в группе 2
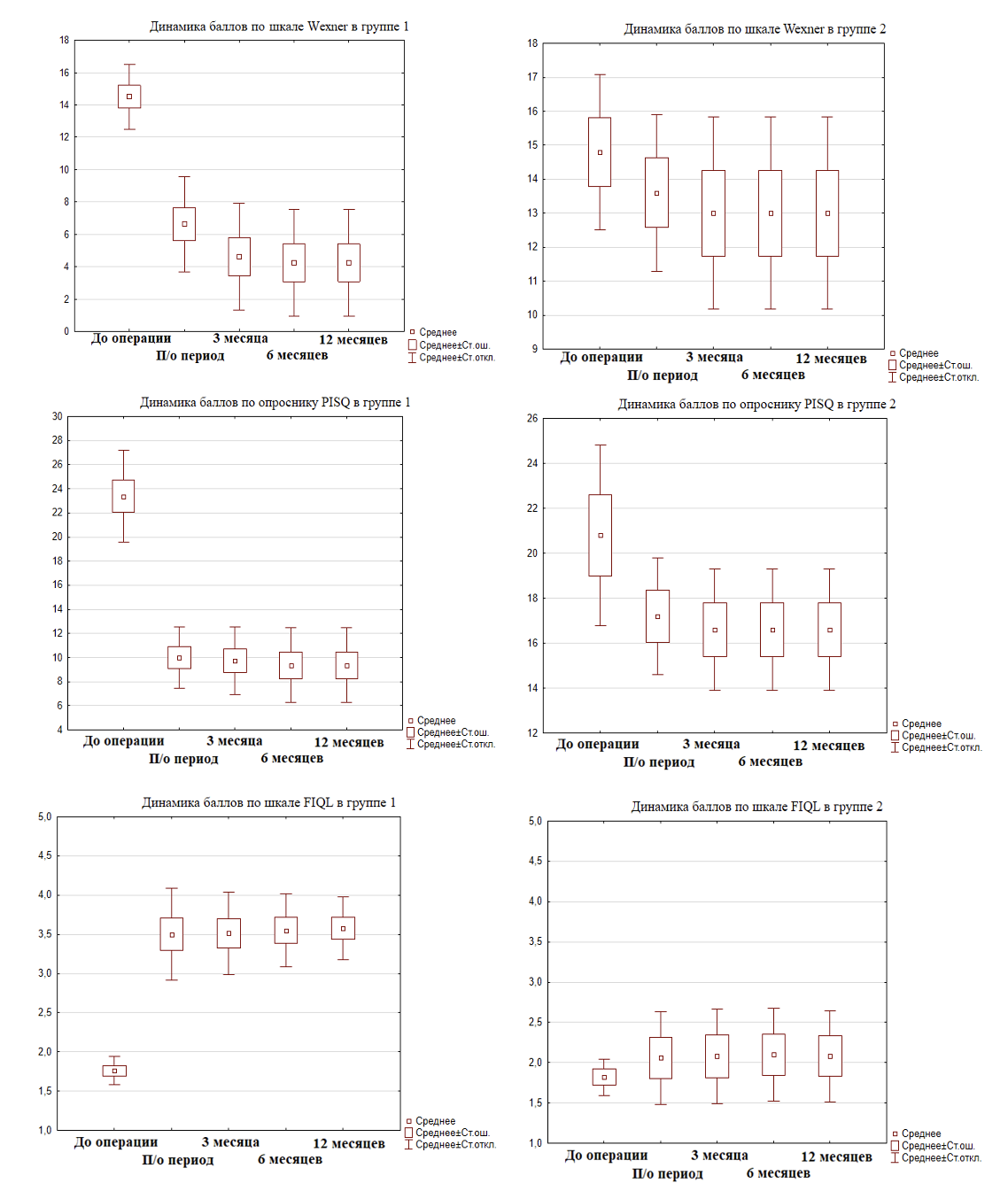
Рис.5. Диаграмма динамики выраженности симптомом по данным опросников и шкал в группах 1 и 2
Таким образом, в первой группе, включавшей пациенток без клинически выявляемого нарушения структуры сфинктерного аппарата анального канала, сакральная нейростимуляция продемонстрировала высокую эффективность: улучшение по шкале Wexner составило в среднем 70%, по опроснику PISQ — 60%, а по показателю FIQL — 51%.
Во второй группе, где имелся разрыв сфинктера, динамика была выражена значительно слабее. Ни одна из пациенток не достигла порога улучшения ≥50%, а средние показатели изменения симптомов распределились следующим образом: улучшение по Wexner — 13%, по PISQ — 21%, по FIQL — 12,5%. Статистическую значимость удалось подтвердить лишь для показателей сексуальной функции; различий по степени инконтиненции и качеству жизни выявлено не было.
При этом важно учитывать, что часть пациенток с разрывом сфинктера ранее перенесли сфинктеропластику с недостаточным результатом, а повторное вмешательство им не показано, либо изначально реконструктивная операция не являлась оптимальным вариантом. В подобных случаях сакральная нейростимуляция может выступать фактически единственным доступным методом уменьшения выраженности энкопреза и повышения качества жизни. Следует подчеркнуть, что данные о долгосрочной эффективности SNRS у пациентов этой категории пока ограничены.
Обсуждение
Механизмы воздействия электростимуляции крестцовых корешков до конца не изучены, что во многом связано с её эффективностью при клинически различающихся состояниях — от энкопреза до проктогенных запоров [4]. Считается, что воздействие SNRS реализуется через многоуровневую нейромодуляцию: стимуляция влияет как на сегментарные структуры спинного мозга, так и на супраспинальные центры, что приводит к перестройке нисходящей регуляции аноректальной функции. Предполагается, что терапевтический эффект обусловлен не прямой активацией или подавлением отдельных нервных путей, а восстановлением баланса между симпатическим и парасимпатическим звеньями вегетативной иннервации.
Существовали предположения, что наличие повреждения сфинктерного аппарата может снижать эффективность нейромодуляции, однако данные ряда исследований опровергли эту точку зрения [4]. Тем не менее в нашем анализе пациенты с разрывом сфинктера демонстрировали существенно более скромный ответ на лечение, что подчёркивает важность анатомической сохранности сфинктерного комплекса.
Отдалённые результаты нейромодуляции выглядят весьма многообещающими: систематические обзоры с длительностью наблюдения более трёх лет показывают, что улучшение контроля дефекации и снижение выраженности симптомов сохраняются у большинства пациентов, параллельно удерживается и высокий уровень качества жизни [9]. На фоне таких данных закономерно возникает интерес к оптимальным срокам проведения операции после появления первых симптомов. При этом следует учитывать, что в перспективе возможны повторные вмешательства, связанные, например, с заменой генератора или необходимостью коррекции положения электрода при его миграции [10].
Несмотря на необходимость периодических проверок, SNRS остаётся надёжным, малотравматичным и реверсивным методом, который способен заменить более инвазивные операции или служить их дополнением. Перспективные исследования должны быть направлены на оценку отдалённых результатов и сравнение эффективности SNRS с сфинктеропластикой при различных анатомических вариантах повреждений сфинктера. В целом, стимуляция сакральных корешков значительно расширяет возможности лечения послеродовых повреждений сфинктерного комплекса, снижает выраженность энкопреза, уменьшает болевой синдром и улучшает качество жизни пациенток [11].
Отдельного внимания заслуживают клинические наблюдения во время тестового периода. Уже к концу первой–второй недели стимуляции обычно отмечается уменьшение эпизодов каломазанья, улучшение чувства наполнения прямой кишки, восстановление нормального позыва и удержание стула плотной консистенции. Однако способность удерживать мягкий и жидкий стул, а также газы, формируется, как правило, лишь ко второй–третьей месяцу стимуляции. Учитывая, что длительный тестовый период существенно повышает риск инфекционных осложнений, его применение у пациенток, жалобы которых ограничиваются недержанием жидкого стула и газов, представляется малоцелесообразным.
Кроме того, высокая эффективность стимуляции у женщин без анатомического дефекта сфинктера ставит под сомнение необходимость проведения полноценного тестового этапа и для этой категории пациенток.
Ограничениями настоящего исследования следует считать небольшое число включённых пациенток, сравнительно короткий период наблюдения, отсутствие универсальных и полностью объективных инструментов оценки выраженности инконтиненции, а также ретроспективный дизайн, который накладывает методологические ограничения на интерпретацию результатов.
Заключение
Сакральная нейростимуляция (SNRS) демонстрирует значительный терапевтический потенциал в коррекции энкопреза у женщин с послеродовыми повреждениями анального сфинктера. Согласно полученным данным, у пациенток без разрыва сфинктерного комплекса нейромодуляция обеспечивает выраженное улучшение состояния: снижение выраженности симптомов составляет в среднем 70% по шкале Wexner, 60% по опроснику PISQ и 51% по показателю FIQL.
У пациенток же с установленным разрывом анального сфинктера положительная динамика менее заметна — улучшение достигает 13% по Wexner, 21% по PISQ и 12,5% по FIQL. Эти результаты позволяют рассматривать SNRS как ведущий метод лечения послеродовой анальной инконтиненции при отсутствии дефекта сфинктера, а при наличии анатомических нарушений — как дополнительную или альтернативную опцию, особенно в ситуациях, когда сфинктеропластика технически невозможна или её результаты оказались неудовлетворительными.
Для повышения эффективности нейромодуляции требуется тщательный сбор анамнеза и детальная клиническая оценка. Принимая во внимание высокую успешность SNRS у пациенток без структурного повреждения сфинктерного аппарата, а также низкую информативность длительного тестового периода у женщин с недержанием жидкого стула и газов, целесообразно рассматривать возможность имплантации постоянной системы без проведения предварительного тестового этапа в указанных клинических группах.
1. Sultan AH, Kamm MA, Hudson CN, Bartram CI. Anal sphincter disruption during vaginal delivery. N Engl J Med. 1993;329(26):1905–1911. https://doi.org/10.1056/NEJM199312233292601
2. Orlando A, Thomas G, Murphy J, Hotouras A, Bassett P, Vaizey C. A systematic review and a meta-analysis on the incidence of obstetric anal sphincter injuries during vaginal delivery. Colorectal Dis. 2024;26(2):227-242. doihttps://doi.org/10.1111/codi.16831 EDN: https://elibrary.ru/BOCCFQ
3. Meyer, I., & Richter, H. E. (2016). Evidence-Based Update on Treatments of Fecal Incontinence in Women. Obstetrics and gynecology clinics of North America, 43(1), 93–119. https://doi.org/10.1016/j.ogc.2015.10.005
4. Leo CA, Thomas GP, Bradshaw E, et al. Long-term outcome of sacral nerve stimulation for faecal incontinence. Colorectal Dis. 2020;22(12):2191-2198. doihttps://doi.org/10.1111/codi.15369 EDN: https://elibrary.ru/UTGTOL
5. Matzel KE, Lux P, Heuer S, Besendörfer M, Zhang W. Sacral nerve stimulation for faecal incontinence: long-term outcome. Colorectal Dis. 2009;11(6):636-641. doihttps://doi.org/10.1111/j.1463-1318.2008.01673.x
6. Dudding TC, Parés D, Vaizey CJ, Kamm MA. Predictive factors for successful sacral nerve stimulation in the treatment of faecal incontinence: a 10-year cohort analysis. Colorectal Dis. 2008;10(3):249-256. doihttps://doi.org/10.1111/j.1463-1318.2007.01319.x
7. Wexner SD, Coller JA, Devroede G, et al. Sacral nerve stimulation for fecal incontinence: results of a 120-patient prospective multicenter study. Ann Surg. 2010;251(3):441-449. doihttps://doi.org/10.1097/SLA.0b013e3181cf8ed0
8. Eggers E, Crouss T, Beausang J, et al. Long-term Outcomes of Sacral Nerve Stimulation on the Treatment of Fecal Incontinence: A Systematic Review. Neuromodulation. Published online August 17, 2024. doihttps://doi.org/10.1016/j.neurom.2024.06.504 EDN: https://elibrary.ru/PYQIVB
9. Mellgren A, Wexner SD, Coller JA, et al. Long-term efficacy and safety of sacral nerve stimulation for fecal incontinence. Dis Colon Rectum. 2011;54(9):1065-1075. doihttps://doi.org/10.1097/DCR.0b013e31822155e9
10. Tan E, Ngo NT, Darzi A, Shenouda M, Tekkis PP. Meta-analysis: sacral nerve stimulation versus conservative therapy in the treatment of faecal incontinence. Int J Colorectal Dis. 2011;26(3):275-294. doihttps://doi.org/10.1007/s00384-010-1119-y EDN: https://elibrary.ru/ULZRIR
11. Tjandra JJ, Chan MK, Yeh CH, Murray-Green C. Sacral nerve stimulation is more effective than optimal medical therapy for severe fecal incontinence: a randomized, controlled study. Dis Colon Rectum. 2008;51(5):494-502. doihttps://doi.org/10.1007/s10350-007-9103-5




